Coronavirus y la carrera para encontrar una vacuna
Casi al mismo tiempo que la pandemia de coronavirus comenzaba a traspasar fronteras como un tsunami imparable, laboratorios de todo el mundo iniciaban una carrera contra reloj para encontrar una vacuna que pueda contrarrestar al nuevo patógeno. No es el único recurso científico para detener al virus, pero sí el más importante. Las investigaciones siempre parten de la premisa de que el desarrollo de vacunas se caracteriza por un alto nivel de fracaso, pero nunca antes la comunidad científica internacional había actuado tan coordinadamente ni con tantos recursos para solucionar un problema.
Los contagios declarados en todo el mundo superan los 61 millones, mientras que los fallecimientos sobrepasan ya los 1,4 millones, según los datos que recopila la Universidad Johns Hopkins. Hallar una vacuna contra el nuevo coronavirus se ha convertido en una cuestión de máxima prioridad. Repasamos algunos de los puntos más importantes que caracterizan a este gran reto científico:
¿Por qué es importante una vacuna contra el coronavirus?
Hasta que no se encuentre una vacuna efectiva, el coronavirus SARS-CoV-2 podrá circular libremente por las personas, que estarán expuestas al patógeno. El nuevo virus ha demostrado una capacidad de contagio superior a la que en un principio se estimó, lo que le ha permitido propagarse a lo largo y ancho del mundo de una manera explosiva.
Medidas como la higiene, el uso de mascarillas o el distanciamiento físico seguirán siendo muy efectivas, y pueden frenar el ritmo de contagios hasta niveles de relativa seguridad, pero el regreso a la situación anterior a la pandemia va a depender del hallazgo de soluciones terapéuticas. Dentro de estas, la vacuna es, con mucha diferencia, la más importante.
¿Se trata solo de desarrollar una vacuna?
La frenética carrera por encontrar una vacuna tiene ante sí un triple desafío titánico. Primero, para acortar los plazos debe conseguir acelerar esa relativa lentitud que caracteriza al proceso de desarrollo, aunque garantizando en todo momento la seguridad del fármaco. Pero también hay que considerar que la vacuna realmente exitosa no tiene que ser solo efectiva, sino que además debe poder producirse a una escala nunca antes conocida -varios miles de millones de unidades en el menor tiempo posible-, por lo que la implicación de la industria farmacéutica es fundamental. El tercer paso sería asegurar unas campañas masivas de vacunación también inéditas a nivel mundial.
¿Cuánto se tarda habitualmente en desarrollar una vacuna?
El proceso se está acelerando al máximo, pero hay fases que no pueden ser más rápidas, y requieren de meses de pruebas precisamente para garantizar esa seguridad que siempre acompaña a las vacunas. En un contexto de pandemia, pueden parecer siglos, pero hay que tener en cuenta que en condiciones normales el desarrollo de una vacuna se extiende durante varios años e incluso décadas.
Como consecuencia de la exigencia extrema que acompaña al desarrollo de vacunas, los investigadores suelen seguir un proceso lineal en el que cada evidencia se analiza hasta el mínimo detalle antes de dar el siguiente paso. Pero ahora los procesos de investigación arrancan lo antes posible y muchas fases se ejecutan en paralelo, abandonando el esquema lineal. Aunque hay que tener claro que las fases no se están acortando, simplemente se están superponiendo. También, es muy importante el hecho de que cualquiera de estos proyectos cuenta con una financiación impensable en otro momento, por lo que estas vacunas experimentales se ahorran una de las partes más engorrosas que habitualmente ralentiza el proceso.
Otra de las medidas más importantes para acortar los plazos es la de la "revisión continua" por parte de las autoridades sanitarias. La Agencia Europea del Medicamento (EMA) ya está utilizando este procedimiento con las vacunas experimentales de Pfizer y AstraZeneca. De esta manera, se analiza el fármaco desde "el primer lote de datos" de estudios de laboratorio, en lugar de al final del proceso, como se hace habitualmente.
En todo caso, esta mayor rapidez no se va a traducir en una menor seguridad. Las agencias reguladoras de medicamentos garantizarán que las futuras vacunas no produzcan efectos adversos graves en las personas a las que se administra.
¿Cuántas fases debe superar una vacuna?
Antes de cualquier prueba clínica en humanos, el candidato a vacuna debe superar una Fase 0 o preclínica, que incluye pruebas in vitro y en animales. La vacuna debe demostrar que es segura y que funciona en los organismos animales. Si lo hace, puede pasar al estudio clínico en seres humanos, que se divide a su vez en tres fases, con una cuarta adicional una vez que el fármaco ya esté autorizado y comercializado:
- Fase 1: La vacuna se prueba en pequeños grupos de entre 20 y 100 personas sanas. El estudio se centra en confirmar que es segura y la clase de respuesta inmune que genera, identificando ya posibles efectos secundarios y determinando la dosis adecuada.
- Fase 2: Es un estudio a mayor escala en el que participan varios cientos de personas. Aquí se evalúan los efectos secundarios más comunes en el corto plazo y cómo evoluciona el sistema inmune.
- Fase 3: Es un ensayo mucho más grande en el que participan varios miles de voluntarios, que ya se exponen al virus. Existe un grupo de control, al que se le administra placebo, y se compara cómo evolucionan las personas que fueron vacunadas respecto a las que no, al mismo tiempo que se recolectan datos estadísticos acerca de la eficacia y la seguridad. También sirve para detectar otros posibles efectos secundarios que hayan pasado desapercibidos en la fase 2.
- Fase 4: Las vacunas se someten a una nueva fase de evaluación después de que hayan sido sido aprobadas y comercializadas. El objetivo es seguir recabando información que pueda reforzar su seguridad y eficacia, con una muestra mucho mayor de personas. Aquí pueden aparecer efectos adversos que no se han visto en fases anteriores, precisamente porque son menos frecuentes.
Desde que la OMS declaró el brote de coronavirus como pandemia, los proyectos de vacuna se han multiplicado en todo el planeta. AFP
¿Qué proyectos destacados de vacuna existen a nivel mundial?
Desde que la Organización Mundial para la Salud (OMS) declaró el brote de coronavirus como pandemia, los proyectos de vacuna se han multiplicado en todo el planeta. Con fecha 12 de noviembre, la última referencia en la que aporta datos, el organismo internacional reconoce 164 proyectos que ya han encontrado un candidato a vacuna y se encuentran en fase preclínica. Además, hay otros 48 que la han superado y han alcanzado la etapa clínica, con pruebas en humanos. De ellos, once están en la fase 3, previa a la comercialización:
- Instituto Jenner de la Universidad de Oxford (Reino Unido). Fase 3: En este proyecto, el más importante que se está llevando a cabo en suelo europeo, también participa la farmacéutica AstraZeneca. Utiliza una versión atenuada del virus del resfriado común de los chimpancés, que se caracteriza por su seguridad.
Esta vacuna experimental previene la COVID-19 en un 70,4% de los casos, aunque llega a alcanzar un 90% en algunas dosificaciones, según indican los resultados preliminares de la fase 3 del ensayo clínico. Sobre esta disparidad de porcentajes, la Universidad de Oxford y AstraZeneca han anunciado que someterán a la vacuna a un "estudio adicional" para despejar dudas sobre su eficacia.
Si finalmente esta vacuna experimental demuestra su seguridad y eficacia, podría estar ya disponible para finales de este año, puesto que una parte de su producción se inició en paralelo a las pruebas clínicas. La Comisión Europea (CE) firmó un contrato con AstraZeneca para el suministro de 400 millones de dosis, destinadas a la población de la UE. España se ha asegurado al menos 30 millones de dosis, de las que podría recibir una partida inicial de tres millones este mismo mes de diciembre.
- BioNTech / Pfizer (Alemania / Estados Unidos). Fase 3: Las farmacéuticas Pfizer y BioNTech han anunciado que su vacuna experimental ha concluido la fase 3 de ensayos clínicos con una eficacia del 95% a partir de los 28 días después de la primera dosis, según un comunicado de las propias compañías, quienes ya emitieron una evaluación preliminar hace poco más de una semana que situaba esta efectividad aproximadamente en un 90%. Ahora, tras los resultados de este análisis final, pedirán su aprobación de emergencia a la agencia del medicamento de Estados Unidos (FDA) y a otras agencias, como la de la Unión Europea (EMA).
Este candidato a vacuna se ha desarrollado a partir de cuatro variantes, basadas todas ellas en ARN mensajero sintético. Este enfoque múltiple permite realizar una evaluación simultánea para aumentar las posibilidades de éxito.
- Moderna (Estados Unidos), Fase 3: Esta vacuna está basada en ARN mensajero combinado con el código genético del virus, y España participará en su proceso de producción. Se encuentra ya en fase 3 de ensayos clínicos. La farmacéutica estadounidense acaba de anunciar que tiene una eficacia del 94,5%, según un análisis intermedio realizado por la propia compañía. La biotecnológica solicitará ahora una autorización de emergencia para su uso en Estados Unidos en "las próximas semanas".
- Janssen / Johnson & Johnson (Estados Unidos). Fase 3: Janssen, propiedad del gigante Johnson & Johnson, tuvo que detener los ensayos de su vacuna en fase 3 de investigación debido a una "enfermedad inexplicable" en un participante. Las pruebas se reanudaron once días después y, a pesar del retraso, la empresa espera obtener resultados a finales de año.
Su vacuna Ad26.COV2-S está basada en un adenovirus recombinante no replicativo que es capaz de generar una respuesta inmunológica frente a la proteína S del coronavirus (de 'spike', también llamada "espiga" en español). La compañía cree que, de seguir obteniendo los mismos resultados satisfactorios, puede estar en el mercado a principios de 2021. España, que ya estaba participando en la fase 2, acaba de autorizar también la fase 3, en lo que supone el primer ensayo clínico en esta etapa que se lleva a cabo en el país.
- Novavax (Estados Unidos). Fase 3: Después de anunciar que su candidato a vacuna ha mostrado respuesta inmune positiva, mientras que apenas ha provocado efectos secundarios en la mayoría de participantes, la compañía biotecnológica estadounidense inició la fase 3 de las pruebas de este prototipo basado en baculovirus recombinantes.
El grupo biofarmacéutico gallego Zendal, a través de su filial Biofabri, ha sido escogido para producir industrialmente el antígeno de esta vacuna para toda Europa.
- Bharat Biotech (India). Fase 3: Bautizada como 'Covaxine' esta vacuna experimental que se desarrolla en India, uno de los países más castigados por la pandemia, acaba de comenzar la fase 3 de ensayos clínicos. Este candidato se basa en una cepa inactivada del coronavirus SARS-CoV-2, el causante de la enfermedad COVID-19.
- Sinovac (China). Fase 3: Esta propuesta china parte de virus inactivos purificados, y ha generado muchas expectativas. Hace semanas que comenzó la fase 3, después de que Brasil diese el visto bueno para que la compañía inoculase la vacuna experimental a miles de voluntarios del país sudamericano.
Brasil decidió suspender temporalmente los ensayos clínicos tras detectar un "evento adverso grave", aunque después retomó las pruebas una vez que comprobó que el suceso no estaba relacionado directamente con la administración del fármaco.
La vacuna podrá aplicarse masivamente a principios del próximo año, según estimaciones del presidente de la farmacéutica, quien asegura que tienen capacidad para fabricar cerca de 300 millones de dosis al año.
- Sinopharm / Instituto de Productos Biológicos de Wuhan y Sinopharm / Instituto de Productos Biológicos de Pekín (ambos en China). Fase 3: China también está desarrollando estos dos proyectos independientes entre sí y muy prometedores. Ambos se basan en virus inactivados y detrás de ellos está Sinopharm, el gigante farmacéutico de carácter estatal. También se encuentran en la última fase de ensayos clínicos.
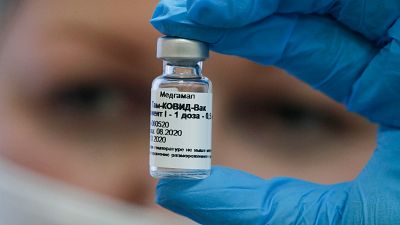
- Gamaleya Research Institute (Rusia). Fase 3: Bautizada con el simbólico nombre de 'Sputnik V', se trata de una vacuna que utiliza como vector un adenovirus humano, y en su desarrollo también participa el Ministerio de Defensa ruso. La OMS ha reconocido la tercera fase de las pruebas clínicas, pero el Gobierno ruso ha autorizado su administración y la da por desarrollada, después de menos de dos meses de pruebas con voluntarios y sin haber completado los ensayos clínicos.
La excesiva rapidez de todo el proceso, sumada a una escasa ortodoxia científica, ha generado muchas sospechas en la comunidad internacional. Recientemente, Moscú ha asegurado que 'Sputnik V' muestra 42 días después de la primera dosis una eficacia de más del 95% y que cada dosis costará menos de 10 dólares.
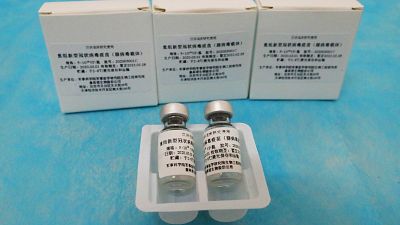
- CanSino Biological Inc. / Instituto de Biotecnologías Pekín (China). Fase 3: Se trata de una vacuna de vector viral. Al ser también de una vacuna de subunidad -una fórmula de nueva generación que no contiene patógenos-, se caracteriza por su seguridad. Debido a las buenas expectativas que está generando, la Oficina Estatal china de Propiedad Intelectual (SIPO, por sus siglas en inglés) ha aprobado su patente, por lo que podría "ser producida en masa en un breve periodo de tiempo". Comenzó a probarse a finales de junio en el Ejército chino. Los resultados de la segunda fase de los ensayos clínicos de la vacuna demostraron que es segura e induce respuesta inmune contra el coronavirus, de acuerdo con una investigación publicada a finales de julio en la revista The Lancet.
- Curevac (Alemania). Fase 2: Esta empresa biofarmacéutica también está desarrollando una vacuna basada en el ARN, que ha obtenido unos resultados muy prometedores en la fase inicial. La Comisión Europea (CE) ha anunciado que está negociando con el laboratorio alemán la compra de 225 millones de dosis de esta potencial vacuna destinadas a la población de la UE.
- Anhui Zhifei Longcom / Instituto de Microbiología (China). Fase 2: Se trata de una vacuna de proteína recombinante, y ya se encuentra en la segunda fase de ensayos clínicos.
- Biological E (India). Fase 1/2. Esta vacuna experimental basada en proteína recombinante, que acaba de comenzar los ensayos clínicos, nació en la Escuela de Medicina de Baylor, en Estados Unidos. Sin embargo, su desarrollo se llevará a cabo en la India, que es una verdadera potencia mundial en el ámbito farmacéutico.
- SpyBiotech / Instituto Serum (India). Fase 1/2. La empresa con sede en Reino Unido SpyBiotech se ha unido al gigante indio Serum para iniciar los ensayos de fase I / II de su vacuna basada en un nuevo virus de partículas (VLP). La vacuna experimental parte de un tratamiento contra la hepatitis B, mediante una tecnología de superpegamento bacteriano que le permite unir antígenos.
- Sanofi Pasteur / GSK (Francia). Fase 1/2: Sanofi Pasteur y GlaxoSmithKline han iniciado las dos primeras fases de los ensayos clínicos de este proyecto de vacuna en diferentes lugares de los Estados Unidos, y prevén concluirlas en diciembre. Si los resultados son satisfactorios, arrancarían la fase 3 ese mismo mes. La vacuna se basa en un antígeno, la proteína S del coronavirus SARS-CoV-2, que se ha desarrollado basándose en ADN recombinante. La secuencia de ADN que codifica este antígeno se ha combinado con el ADN de baculovirus, el mismo en el que Sanofi ha basado una vacuna recombinante contra la gripe.
- Inovio Pharmaceuticals (Estados Unidos). Fase 1/2: Este candidato a vacuna aún está en Fase 1, y comenzó en abril sus ensayos en humanos, basados en el ARN del virus. Se espera que los primeros datos de la respuesta inmune y posibles efectos secundarios se conozcan a finales de verano.
- Beijing Minhai Biotechnology (China). Fase 1/2. Este proyecto chinose basa en virus inactivado, y fue uno de los últimos en incorporarse a la carrera por la vacuna. Acaba ampliar el ensayo clínico, realizando de manera simultánea las fases 1 y 2.
- Instituto de Biología Médica (China). Fase 1/2: El quinto candidato a vacuna que se está investigando en China abre aún más la puerta a la esperanza. Está basado en una versión inactivada del virus.
- Consorcio Genexine (Corea del Sur). Fase 1/2: El primer candidato que llega de Corea del Sur está impulsado por un grupo de seis empresas farmacéuticas, y se trata de una vacuna de ADN.
- Cadila (India). Fase 1/2: Las autoridades sanitarias indias acaban de dar luz verde a la experimentación en humanos de esta vacuna de plásmido de ADN, que llevará a cabo las fases 1 y 2 en un plazo estimado de tres meses. Aún está en fase de reclutamiento de voluntarios.
- Universidad de Osaka / AnGes / Takara Bio (Japón). Fase 1/2: El primer candidato a vacuna que llega de Japón también se basa en ADN y está realizando las fases 1 y 2 de manera simultánea, para ganar tiempo. El proyecto cuenta con el respaldo del Gobierno nipón.
- Kentucky Bioprocessing (Reino Unido / EE.UU.). Fase 1/2. Esta empresa, propiedad de la compañía tabacalera British American Tobacco, ha comenzado recientemente los ensayos en seres humanos de su vacuna experimental desarrollada a base de plantas de tabaco. La compañía ya ha usado una técnica similar para desarrollar un medicamento contra el ébola.
- Arcturus / Duke-NUS (Estados Unidos / Singapur). Fase 1/2. La compañía californiana Arcturus y la Facultad de Medicina Duke-NUS de Singapur han comenzado los ensayos clínicos de su candidato a vacuna denominado LUNAR-COV19, que combina ARNm autorreplicante con LUNAR, un sistema patentado de administración de nanopartículas.
- Instituto de Investigación de Asuntos de Seguridad Biológica (Kazajistán). Fase 1/2. Después de concluir el estudio preclínico con resultados satisfactorios, Kazajistán ha iniciado simultáneamente las dos primeras fases del ensayo en humanos de su vacuna experimental inactivada contra la COVID-19.
- Symvivo (Canadá). Fase 1. Este proyecto está basado en una píldora con bacterias modificadas genéticamente que producen la proteína viral Spike después de pasar por el intestino.
- Instituto Finlay de Vacunas (Cuba). Fase 1. Nueva vacuna experimental que llega de Cuba, que ha sido bautizada como 'SOBERANA 02'. De esta manera, el país caribeño ya está probando dos en fase clínica. Tal y como han explicado los propios investigadores cubanos, la novedad de este segundo proyecto es que se trata de una "vacuna conjugada", en la cual el antígeno del virus "está enlazado químicamente al toxoide tetánico", para que la inmunidad alcance la mucosa del tracto respiratorio y así evite la entrada del virus. Este candidato vacunal podría estar destinado a población pediátrica.
- Instituto de Investigación Biológica de Israel / Instituto Weizmann (Israel). Fase 1. Bautizada como ‘BriLife', se trata de la primera vacuna experimental autorizada por Israel para su administración en humanos. Se basa en el virus de la estomatitis vesicular (VSV) y ya ha sido probada con éxito en animales.
- Merck Sharp & Dohme / IAVI (Estados Unidos). Fase 1. Este candidato se basa en la tecnología del virus de la estomatitis vesicular recombinante (rVSV), empleada contra el virus del ébola-Zaire por la farmacéutica Merck para desarrollar la primera vacuna contra el ébola aprobada para su uso en humanos. Para desarrollar la nueva vacuna contra la COVID-19, MSD se ha aliado con la Iniciativa Internacional para la Vacuna del Sida (IAVI, por sus siglas en inglés), una organización dedicada al desarrollo de medicamentos y vacunas a precios bajos cuyo principal financiador es la Fundación Bill y Melinda Gates
- ImmunityBio & NantKwest (Estados Unidos). Fase 1. Esta vacuna experimental, llamada hAd5, se basa en un adenovirus modificado genéticamente para presentar dos proteínas del coronavirus SARS-CoV-2 (no solo la famosa proteína S), capaces de desencadenar una respuesta inmune que proteja contra futuras infecciones de COVID-19.
- Universidad Ludwig-Maximilians de Munich (Alemania). Fase 1.
- COVAXX (EEUU). Fase 1. Bajo el nombre UB-612, este prototipo se basa en tecnología sintética, es decir, está fabricada en laboratorio a partir de un péptido que imita la estructura de proteínas del coronavirus, por lo que ofrece mayor seguridad.
- Hospital Universitario de Tübingen (Alemania). Fase 1. Se trata de una vacuna experimental basada en péptidos para prevenir la infección por COVID-19
- Instituto Finlay de Vacunas (Cuba). Fase 1. Cuba ha dado luz verde a los ensayos clínicos de su propia vacuna contra el coronavirus SARS-CoV-2, que se prolongarán hasta inicios de 2021. Se llamará 'SOBERANA 01' y se aplicará en dos dosis inyectadas por vía intramuscular. El centro estatal ha fijado en el 11 de enero de 2021 la fecha de finalización de este estudio.
- ReiThera / LEUKOCARE / Univercells (Italia / Alemania / Bélgica). Fase 1. Esta candidata a vacuna, conocida como GRAd-COV2, ya ha sido probada con éxito en animales y que se basa en un vector adenoviral. En esta primera fase Se probará en 90 individuos sanos, de los cuales 45 son personas de entre 18 y 55 años, y 45 son mayores de entre 65 y 85 años, de acuerdo con una nota difundida por la Agencia Italiana del Medicamento (AIFA, por sus siglas en italiano).
- Instituto Pasteur / Univ. Pittsburgh / Themis / MSD (Francia / EE.UU. / Austria). Fase 1. Este proyecto emplea un vector de sarampión modificado para que sea capaz de expresar las proteínas del SARS-CoV-2 en su superficie y generar respuesta inmune.
- Imperial College de Londres (Reino Unido). Fase 1: Científicos de la institución británica acaban de comenzar los primeros ensayos clínicos de una posible vacuna contra la COVID-19. Tal y como han explicado, su proyecto presenta una novedad importante: en lugar de usar una parte del virus, “utiliza hebras sintéticas del material genético del virus, el ARN, empaquetado dentro de pequeñas gotas de grasa”. Alrededor de 300 voluntarios sanos recibirán dos dosis de la vacuna en los ensayos clínicos iniciales, para evaluar si es segura y si produce una respuesta inmune efectiva.
- Clover / GSK / Dynavax (China / Reino Unido / EE.UU. ). Fase 1: Nuevo proyecto de vacuna de proteína recombinante, que se basa en un sistema adyuvante diseñado por GlaxoSmithKline (GSK), capaz de mejorar la respuesta inmune del organismo humano. Las pruebas en humanos acaban de comenzar, y los primeros resultados del estudio estarán listos en agosto.
- Ejército Pop. Lib. / Academia Ciencia Militar / Walvax (China). Fase 1: Denominado ARCoV, este proyecto usa tecnología de ARN mensajero, al igual que los desarrollados por Moderna en Estados Unidos. Es la primera vacuna de este tipo que se está probando en humanos en China.
- Instituto de Biotecnología / Academia Ciencia Militar / Ejército Pop. Lib. (China). Fase 1. Nueva vacuna china que ha entrado en ensayos clínicos. En este caso, vectorizada con adenovirus 5 recombinante (Ad5-nCoV).
- Vaxine Pty Ltd / Medytox (Australia / Corea del Sur). Fase 1: El ensayo que acaba de arrancar en el Royal Adelaide Hospital de Australia, el primero de este tipo en el Hemisferio Sur, probará un nuevo candidato llamado COVAX-19, que se basa en una vacuna de proteína recombinante.
- Medicago Inc./ Universidad Laval (Canadá). Fase 1: La empresa biofarmacéutica Medicago, con sede en Quebec, se ha aliado con la Universidad Laval de la misma ciudad y acaban de comenzar las pruebas en humanos de una vacuna basada en partículas recombinantes similares al virus (CoVLP) y un adyuvante. Las CoVLP imitan la estructura del virus SARS-CoV-2, lo que les permite ser reconocidas por el sistema inmune.
- Universidad de Queensland / GSK / Dynavax (Australia). Fase 1: Segundo proyecto de vacuna que se está desarrollando en el país oceánico. Después de superar la fase preclínica con resultados "excelentes", según sus promotores, 120 voluntarios se disponen a recibir las primeras dosis. Se espera que los primeros resultados de las pruebas se publiquen a finales de septiembre.
- Medigen / NIAID / Dynavax (Taiwán / EE.UU.). Fase 1. Nuevo candidato a vacuna de proteína recombinante impulsada por un adyuvante.
- FBRI SRC VB VECTOR, Rospotrebnadzor, Koltsovo (Rusia). Fase 1. Segundo proyecto de vacuna que llega de Rusia, bautizado como EpikVacCorona. Después de mostrar su eficacia en los ensayos preclínicos, acaba de comenzar la fase clínica. Se trata de una vacuna de carácter peptídico que está compuesta de fragmentos de proteínas virales sintetizados de manera artificial.
- West China Hospital / Universidad de Sichuan (China). Fase 1. Esta vacuna experimental que llega de China presenta uno de los enfoques más novedosos. Las proteínas en las que se basa se cultivan dentro de células de insectos, lo que podría acelerar la producción a gran escala.
- Beijing Wantai Biological Pharmacy / Universidad de Xiamen (China). Fase 1. Se trata de la primera vacuna COVID-19 en aerosol nasal aprobada por la Administración Nacional de Productos Médicos de China para ensayos en humanos.
- Vaxart (Estados Unidos). Fase 1. Esta compañía biotecnológica de San Francisco acaba de arrancar los ensayos clínicos de su vacuna recombinante, basada en adenovirus y mucosal, que tiene la peculiaridad de que se administra en tabletas en lugar de inyectarse.
España cuenta con varios proyectos de importante calado científico, aún en fase preclínica. REUTERS
¿En qué situación se encuentran los proyectos españoles?
Un escalón por debajo, aún en fase preclínica, España cuenta al menos con una decena de proyectos que buscan una vacuna desde diferentes perspectivas. Además, la vacuna experimental RUTI, desarrollada por el Hospital Germans Trias i Pujol y fabricada por la farmacéutica Archivel Farma, ha sido la primera que de momento ha recibido la autorización para realizar un ensayo clínico, aunque solo en Argentina.
En cuanto al resto de proyectos, aún en fase preclínica, se trata de los siguientes:
Investigadores del Centro Nacional de Biotecnología (CNB), perteneciente al Consejo Superior de Investigaciones Científicas (CSIC), ya han iniciado los ensayos preclínicos con animales de un candidato a vacuna basado en una modificación de la que se usó contra la viruela.
En concreto, utilizan una cepa muy atenuada del virus Vaccinia (llamado MVA), de la familia del virus de la viruela, como vector viral para insertarle genes del nuevo coronavirus que puedan inducir una respuesta inmune adecuada frente al SARS-CoV-2. El grupo está liderado por Mariano Esteban y Juan García Arriaza. Tras unos primeros resultados esperanzadores, prevén que puedan comenzar los ensayos en humanos a finales de 2020.
En el mismo centro, otro equipo, dirigido por Luis Enjuanes e Isabel Sola, trabaja en crear una vacuna a partir de una reconstrucción genética del propio coronavirus, atenuando y eliminando los genes más virulentos, y conservando aquellos que dan lugar a proteínas capaces de inducir una respuesta inmunitaria eficaz. No prevén comenzar los ensayos clínicos hasta finales de 2020, como pronto.
Un tercer equipo de investigadores del CSIC, dirigido por Vicente Larraga, del Centro de Investigaciones Biológicas Margarita Salas, está buscando una vacuna frente al SARS-CoV-2 basada en ADN recombinante. El grupo ya desarrolló una vacuna de estas características destinada a la leishmaniosis canina. Su previsión es terminar las pruebas preclínicas para finales de año, y comenzar justo después los ensayos en humanos.
La vacuna no es el único recurso científico para frenar al virus, pero sí el más importante. GTRES
Asimismo, hay otros proyectos que se están desarrollando en laboratorios españoles:
- El Instituto de Investigaciones Biomédicas August Pi i Sunyer (IDIBAPS) - Hospital Clínico de Barcelona coordina un proyecto que utiliza ARNm (ácido ribonucleico mensajero) para inducir la producción de anticuerpos frente al SARS-CoV-2. Gracias a métodos computacionales, los investigadores buscan identificar las partes del virus que inducen a la respuesta inmune más efectiva. Su objetivo es entrar en fase de ensayos clínicos este año.
- El proyecto CoviNanoVax, de la Universidad Ramón Llull, busca una vacuna de ARNm (ARN mensajero) basada en nanopartículas poliméricas que actúan como vectores. Así, estas partículas serían capaces de encapsular material genético y transportar la vacuna hasta las células.
- Un consorcio formado por el Instituto de Investigación del Sida IrsiCaixa, el Barcelona Supercomputing Center y el Centro de Investigación en Sanidad Animal del Instituto de Investigación y Tecnología Agroalimentarias busca vacunas mediante VLP (del inglés Virus-Like Particles), que son partículas diseñadas en el laboratorio a partir de la estructura del virus pero sin capacidad infecciosa. Estas VLPs tengan en su superficie la proteína Spike del SARS-CoV-2 para que, cuando se administren, el sistema inmunitario reconozca la proteína del virus y genere respuesta.
- La Universidad de Santiago de Compostela coordina el desarrollo de dos proyectos de vacuna. El primero de ellos se basa en el ARN mensajero, con la particularidad de que emplea vectores peptídicos para el transporte de material genético.
El segundo proyecto, que se lleva a cabo en el Centro Singular de Investigación en Química Biolóxica e Materiais Moleculares (CiQUS), persigue el desarrollo de una vacuna en base a una nueva metodología que induce a que las células fabriquen microesferas capaces de albergar antígenos virales, que a su vez estimularían al sistema inmune.
- La Fundación Miguel Servet - Navarrabiomed lidera el desarrollo de plataformas de vacunas contra el SARS-CoV-2, un proyecto cuya finalidad es mejorar la ingeniería de posibles vacunas. Tiene dos proyectos en marcha. Uno basado en la inoculación de las proteínas del coronavirus mediante un adyuvante, y otro muy innovador que utiliza vectores lentivirales, empleados frecuentemente en terapias contra enfermedades genéticas. Este último se encuentra en fase preclínica y las pruebas en humanos no comenzarían hasta mediados de 2021, si los resultados iniciales son satisfactorios.
- El Instituto Nacional de Investigación y Tecnología Agraria y Alimentaría (INIA) coordina un proyecto liderado por Rafael Blasco que es muy similar al del equipo de Esteban y García Arriaza. El objetivo es utilizar un vector atenuado derivado de la vacuna de la viruela para insertar dos genes del SARS-CoV-2 y obtener así una respuesta inmunitaria completa. Las previsiones más optimistas contemplan que puedan empezar las pruebas en humanos antes de que acabe 2020.
- La Universidad de Zaragoza trabaja con una posible modificación de una vacuna que ya se está desarrollando contra la tuberculosis, llamada MTBVAC. Se encuentra en las fases preclínicas finales, y ahora se está analizando su inmunidad específica frente al SARS-CoV-2.
¿Qué es la “inmunidad de rebaño”?
La "inmunidad colectiva" o "inmunidad de rebaño" proporciona protección indirecta a los individuos no vacunados, y solo se produce cuando se vacuna una parte muy importante de la población, a la que se suman las personas que son inmunes porque han desarrollado anticuerpos tras un contagio previo. Los epidemiólogos calculan que entre el 60% y el 70% de la población necesita ser inmune al virus para alcanzarla. Hay que tener en cuenta que esta es la manera más efectiva para proteger a personas inmunodeprimidas o que, debido a diversas razones como puede ser la edad, su sistema inmunológico no es capaz de contrarrestar al patógeno a pesar de haber sido vacunadas.
Mientras llega la vacuna, existen posturas que abogan por dejar que se infecten las personas sin ningún tipo de control, para generar esta “inmunidad de rebaño”. Lo que proponen, básicamente, es permitir el aumento de casos positivos y de circulación de personas para incrementar la generación de anticuerpos y la creación de una barrera inmunológica. Pero esta estrategia no pasa de ser una idea descabellada, puesto que en la práctica supone una condena segura al colapso sanitario y a la muerte de millones de personas.
En España, los datos arrojados por el estudio de seroprevalencia que ha llevado a cabo el Ministerio de Sanidad son bastante desalentadores en este sentido. Tan solo un 5,2% de la población española habría generado anticuerpos, por lo que esa "inmunidad de rebaño" sin vacuna se antoja como un horizonte extremadamente difícil de alcanzar, sobre todo teniendo en cuenta el elevado coste humano, sanitario y económico que ha implicado un porcentaje tan bajo.










No hay comentarios:
Publicar un comentario